I. Überblick über Natrium-Ionen-Batterien
Natrium-Ionen-Batterien sind ein Batterietyp, der das Laden und Entladen durch die Bewegung von Natriumionen zwischen den positiven und negativen Elektroden abschließt. Das Funktionsprinzip ähnelt dem von Lithium-Ionen-Batterien. Eine Natrium-Ionen-Batterie besteht hauptsächlich aus einer positiven und einer negativen Elektrode.ein Elektrolyt, ASeparatorund einem Stromkollektor. Beim Laden wird Na⁺ aus der positiven Elektrode extrahiert, passiert den Separator und lagert sich in der negativen Elektrode ein, wo es sich mit Elektronen verbindet. Beim Entladen wird Na⁺ aus der negativen Elektrode extrahiert, passiert den Separator und lagert sich in der positiven Elektrode ein, während Elektronen über einen externen Stromkreis von der negativen zur positiven Elektrode übertragen werden. Schließlich findet in der positiven Elektrode eine Redoxreaktion statt, die den natriumreichen Zustand wiederherstellt.
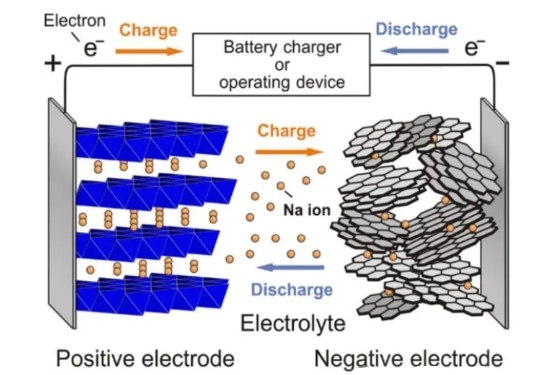
Schematische Darstellung der Ladung und Entladung von Natrium-Ionen-Batterien
II. Drei technische Routen
Im Vergleich zu Lithium-Ionen-Batterien liegt der größte Unterschied bei Natrium-Ionen-Batterien in den Kathodenmaterialien, deren Leistung ebenfalls ein entscheidender Faktor für die Energiedichte, Sicherheit und Lebensdauer der Batterie ist. Natriumionen haben eine größere Masse und einen größeren Radius als Lithiumionen, was zu geringeren Ionendiffusionsraten führt. Dies spiegelt sich in einer etwas geringeren theoretischen Kapazität und Reaktionskinetik der Batterieleistung wider, die Durchbrüche bei den Kathodenmaterialien erfordert, um diese Probleme zu lösen. Derzeit ist der technische Weg für Kathodenmaterialien noch nicht festgelegt, aber Schichtoxide, Preußischblau Analoga, Und Polyanionenverbindungen sindDrei vielversprechende Routen dürften hervorstechen.
ICHII. Schichtoxide
Die allgemeine Formel für Schichtoxide lautet NaxMO2, wobei M für Übergangsmetalle wie Vanadium (V), Chrom (Cr), Mangan (Mn), Eisen (Fe), Kobalt (Co), Nickel (Ni), Kupfer (Cu) usw. steht. Unter diesen sind Mangan (Mn) und Eisen (Fe), die in großen Mengen vorkommen, am häufigsten. Übergangsmetalloxide können weiter in zwei Typen unterteilt werden: Schicht- und Tunnelstrukturen. Bei niedrigem Natriumgehalt (x < 0,5) ist hauptsächlich die Tunnelstruktur vorhanden. Bei relativ hohem Natriumgehalt dominiert im Allgemeinen eine Schichtstruktur mit Na+ zwischen den Schichten, wodurch eine Schichtstruktur entsteht, in der MO2-Schichten und Natriumschichten abwechselnd angeordnet sind.
IV. Berliner Blau-Analoga
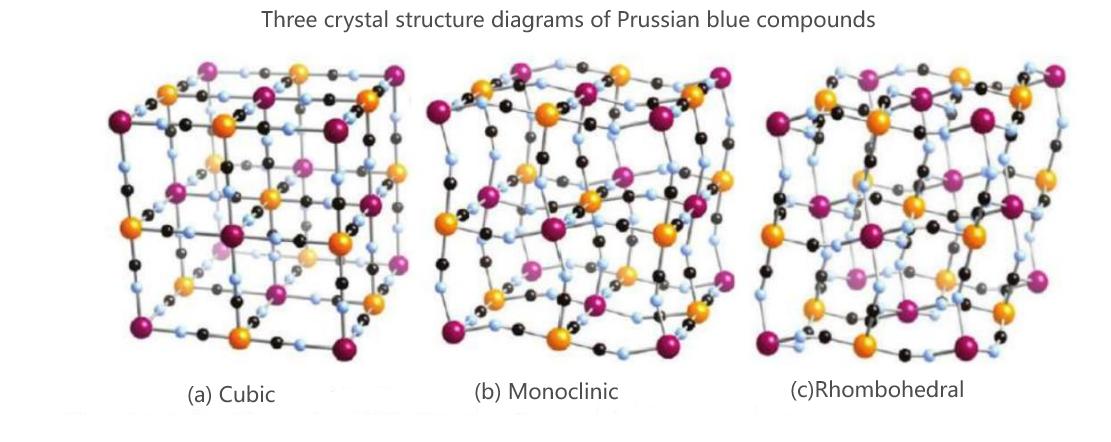
Die allgemeine Formel für Preußischblau-Analoga lautet NaxMA[MB(CN)6]·zH2O. MA und MB stehen für Übergangsmetalle, hauptsächlich Eisen (Fe), Kobalt (Co), Nickel (Ni), Mangan (Mn) usw. Aufgrund ihres einzigartigen offenen Gerüsts und ihrer dreidimensionalen makroporösen Struktur eignen sich Preußischblau-Verbindungen für die Migration und Speicherung von Natriumionen. Eisenbasierte Verbindungen bieten Vorteile.Preußischblau und manganbasiertes Preußischblau haben die Vorteile, dass sie als Rohstoffe reichlich vorhanden, kostengünstig, hochspezifisch und leistungsstark sind sowie eine ausgezeichnete elektrochemische Stabilität aufweisen. Da bei den derzeitigen Produktionsmethoden meist die Mitfällungsmethode zum Einsatz kommt, treten zu den Nachteilen häufig viel Kristallwasser und Strukturdefekte von Fe(CN)6 auf. Das Kristallwasser neigt dazu, die Natriumspeicherplätze und Natriumionen-Deinterkalationskanäle im Kristall zu besetzen, wodurch der Natriumionengehalt im Material sinkt und die Natriumionenmigrationsrate verringert wird. Strukturdefekte und Kristallwasser von Fe(CN)6 können beim Laden und Entladen des Materials zu einem Strukturkollaps führen und so die Zyklenleistung des Materials beeinträchtigen.
Die Herstellungsverfahren für Berliner Blau-Verbindungen umfassen hauptsächlich die Kopräzipitation und die Hydrothermalsynthese. Die Kopräzipitation ist dabei die am weitesten verbreitete Methode, da sie die Vorteile eines einfachen Herstellungsprozesses, keiner Hochtemperaturbehandlung und der einfachen Gewinnung phasenreiner Produkte bietet. Allerdings ist die Kopräzipitation derzeit noch mit zwei Problemen behaftet. Erstens ist die Herstellungszeit lang und zweitens ist die Ausbeute gering. Die Hydrothermalsynthese weist viele Gemeinsamkeiten mit der Kopräzipitation auf. Sie bietet die Vorteile einer kurzen Reaktionszeit und einer gleichmäßigen Verteilung der Materialpartikel. Allerdings weist die Hydrothermalsynthese derzeit drei Nachteile auf. Erstens findet der Reaktionsprozess in einem geschlossenen System statt und kann nicht direkt beobachtet werden. Zweitens sind Hochtemperatur- und Hochdruckschritte erforderlich, die hohe Anforderungen an die Produktionsanlagen stellen. Drittens ist das Verfahren umständlich und für die industrielle Produktion ungeeignet.
V. Polyanionische Verbindungen
Die allgemeine Formel polyanionischer Verbindungen lautet NaxMy[(XOm)n-]z, wobei M ein Metallion mit variabler Valenzstufe und X Elemente wie P, S und V sind. Die Vorteile sind gute Stabilität, Zyklenfestigkeit und Sicherheit, jedoch auch die geringe spezifische Kapazität und die schlechte Leitfähigkeit. Je nach Struktur werden sie in Olivinphosphate, NASCICON-Verbindungen (Na+-Schnellionenleiter) und Phosphatverbindungen eingeteilt.
Die Herstellung von NaFePO4 mit Olivinstruktur als Kathodenmaterial für Natrium-Ionen-Batterien ähnelt der von Lithiumeisenphosphat. Die theoretische Kapazität beträgt 154 mAh/g, die Betriebsspannung 2,9 V. Allerdings ist die elektrische Leitfähigkeit relativ gering und es gibt nur eindimensionale Na+-Diffusionskanäle, was die Leistung beeinträchtigt. Derzeit wird die elektrische Leitfähigkeit durch Kohlenstoffbeschichtung oder Ionensubstitution verbessert. NaFePO4-Verbindungen mit NaSCI-Struktur sind schnelle Ionenleiter mit einer theoretischen spezifischen Kapazität von ca. 120 mAh/g und einer Betriebsspannung von ca. 3,3 V. Sie zeichnen sich durch eine dreidimensionale Gerüststruktur, eine hohe Ionendiffusionsrate sowie eine gute kinetische und Zyklenstabilität aus. Die Einführung von fünfwertigem V ist jedoch häufig toxisch und stellt eine große Gefahr für die menschliche Gesundheit dar, was den großflächigen Einsatz teilweise einschränkt.
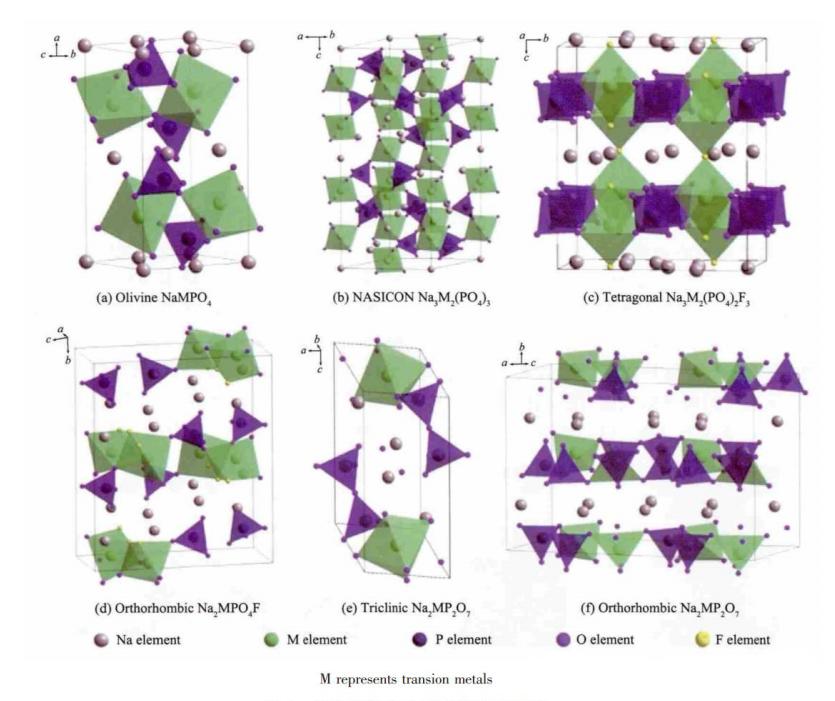
Kristallstrukturen verschiedener polyanionischer Kathodenmaterialien











